サイト内検索
分子研について
研究情報
共同利用案内
- 共同研究・施設利用案内
- 申請概要
- 共同研究受入研究室・利用装置一覧
- WEB申請
大学院
- 大学院教育
- 大学院案内
- 受験生向け情報
- 他大学の学生の受け入れ
- 在校生向け情報
お知らせ
2015/05/28
プレスリリース
藤田 誠 (東京大学大学院工学系研究科応用化学専攻 教授)
加藤 晃一(自然科学研究機構 岡崎統合バイオサイエンスセンター/分子科学研究所 教授)
佐藤 宗太(東北大学原子分子材料科学高等研究機構 准教授)
アルツハイマー病など神経変性疾患の発症の引き金となるのは、神経細胞膜の上で高密度に集まってクラスター化した糖脂質(糖鎖クラスター)が、凝集性タンパク質を捕まえる現象であることがわかってきています。アルツハイマー病の原因物質であるアミロイドβという凝集性タンパク質は、神経系に豊富に存在する糖脂質であるGM1ガングリオシドのクラスターによって認識され、選択的に捕捉されます。その後、疎水性細胞膜中に折りたたんで埋め込まれたタンパク質が核となってアミロイド線維が成長することが明らかになっています。しかし、糖鎖クラスターが、どのようにしてタンパク質を選択認識するのか、その詳細な機構はわかっていませんでした。
今回、東京大学 大学院工学系研究科 応用化学専攻の藤田 誠教授と自然科学研究機構 岡崎統合バイオサイエンスセンター/分子科学研究所の加藤晃一教授、東北大学 原子分子材料科学高等研究機構の佐藤宗太准教授らの研究グループは、自己組織化の手法をつかって、精巧に分子デザインされた糖鎖クラスターをつくりだすことに成功しました。有機分子と遷移金属イオンとの自己組織化をつかうと、一義構造(注2)をもつ世界最大級の球状分子を、原料を混ぜるだけで効率的に構築できます。(参照:過去の東大からのプレスリリース www.u-tokyo.ac.jp/content/400008759.pdf)。
本研究グループは、生物由来の糖鎖を人工合成した自己組織化超分子とハイブリッド化し、サイボーグ超分子をうみだすことに成功しました。凝集性タンパク質は疎水性の部位があると捕捉されてしまうので、糖鎖クラスター部分との結びつきを観測できなくなってしまいます。そこで、本研究グループは、疎水性の細胞膜に相当する部位がない球状分子に、GM1ガングリオシドに含まれる疎水性部分を切除した上で糖鎖だけを連結する工夫をしました。このような分子設計にもとづいて、糖鎖の数や位置・表面の曲率といったクラスターとしての構造が厳密に制御された、GM1糖鎖クラスターをつくりだしました(図1)。この糖鎖クラスターをアミロイドβタンパク質と混合し、核磁気共鳴(NMR)による解析を行ったところ、タンパク質のN末端を選択的に認識する様相がわかりました。また、パーキンソン病の発症に深く関わっているα-シヌクレインタンパク質の認識機構が明らかになりました。生体内糖鎖クラスターを、その生体機能を保持したまま構造が明確な人工分子に移植することで、高分解能な解析を実現できる分子の開発に至り、未知の生命現象の機構に迫ることができました。
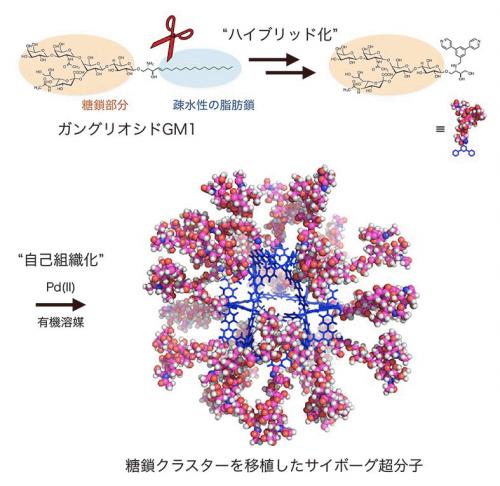 図1 生物由来の糖鎖(表面の赤と白の部分)が、人工合成された球状分子(中心の青い部分)にハイブリッド化して連結された、サイボーグ超分子の合成方法。ガングリオシドGM1に含まれる疎水性部位を切り離した上で、球状錯体の上に連結しています。
図1 生物由来の糖鎖(表面の赤と白の部分)が、人工合成された球状分子(中心の青い部分)にハイブリッド化して連結された、サイボーグ超分子の合成方法。ガングリオシドGM1に含まれる疎水性部位を切り離した上で、球状錯体の上に連結しています。
本研究グループは、精巧につくられたサイボーグ超分子をつかって、病因物質であるタンパク質が細胞表面でどのように捕らえられているのか、詳細に明らかにすることに成功しました。このサイボーグ超分子は、生命に由来する分子や人工合成された分子など、さまざまな分子を自在に移植することで、使用目的に合わせた自由な分子設計ができます。今後、発病のメカニズムを調べる解析ツールとしてつかわれることが期待されます。さらに、病因物質を吸着して除去するように設計することで、創薬や治療へと応用されることが期待されます。
なお本研究は、JST, ACCEL、科研費(新学術領域研究「動的秩序と機能」等)、およびナノプラット(分子研)の研究助成を受けて行われました。
雑誌名: Angew. Chem. Int. Ed. (Angewandte Chemie International Edition、ドイツ化学会誌)
論文タイトル:Self-Assembled Spherical Complex Displaying a Gangliosidic Glycan Cluster Capable of Interacting with Amyloidogenic Proteins
著者:Sota Sato*1,3, Yutaka Yoshimasa1, Daishi Fujita1, Maho Yagi-Utsumi2, Takumi Yamaguchi2, Koichi Kato*2, and Makoto Fujita*1
1. 東京大学大学院工学系研究科応用化学専攻:佐藤宗太(研究当時所属)、吉正泰、藤田 大士、藤田 誠
2. 自然科学研究機構岡崎統合バイオサイエンスセンター生命動秩序形成研究領域・生命分 子研究部門:矢木-内海真穂、山口拓実、加藤晃一
3. 東北大学原子分子材料科学高等研究機構:佐藤宗太(現所属)
DOI番号: 10.1002/anie.201501981
佐藤 宗太(さとう そうた)
東北大学 原子分子材料科学高等研究機構 准教授
電話:022-217-6160、FAX:022-217-6233、メール:satosota@m.tohoku.ac.jp
藤田 誠(ふじた まこと)
東京大学 大学院工学系研究科 応用化学専攻 教授
電話:03-5841-7259、FAX:03-5841-7257、
メール:mfujita@appchem.t.u-tokyo.ac.jp
加藤 晃一(かとう こういち)
自然科学研究機構 岡崎統合バイオサイエンスセンター/分子科学研究所 教授
電話:0564-59-5225、FAX:0564-59-5224、メール:kkatonmr@ims.ac.jp
注1:サイボーグ超分子
生体内で生命活動を担っているパーツを、その生体機能を保ったまま人工分子に組み込んでつくった分子をサイボーグ超分子と名付けている。有機合成の手法を用いることで、目的に応じて生体由来の分子を移植することができ、たとえば今回の成果では、不要な疎水性部位をガングリオシドGM1から切除して、必要な糖鎖部位だけを球状分子に連結できた。一義構造を有する超分子であるために、本来の分子システムがもつ密集構造や柔軟性のある構造を精密に保持することが可能となり、生体機能を人工システムに導入し制御できる特徴がある。
注2:一義構造
全体の構造を構成するユニットの数や集まり方が厳密に決まっており、かたち、大きさ、重さ(分子量)にいっさい分布をもたない、厳密に定まった分子構造体のこと。