サイト内検索
分子研について
研究情報
共同利用案内
- 共同研究・施設利用案内
- 申請概要
- 共同研究受入研究室・利用装置一覧
- WEB申請
大学院
- 大学院教育
- 大学院案内
- 受験生向け情報
- 他大学の学生の受け入れ
- 在校生向け情報
お知らせ
2017/04/11
プレスリリース
|
名古屋大学大学院医学系研究科(研究科長 門松健治)機能分子制御学の澤口翔伍大学院生、小川光貴研究員、岡島徹也教授らの研究グループは、米国アルバート・アインシュタイン医科大学のPamela Stanley教授と自然科学研究機構 岡崎統合バイオサイエンスセンターの加藤晃一教授らの研究グループとの共同研究で、Notch受容体※1の糖修飾として知られているO-結合型N-アセチルグルコサミン(以下、O-GlcNAc※2)が、Notch受容体のリガンドの1つであるDelta-likeによるNotchシグナルの活性化を促進することを明らかにしました。
糖によるタンパク質の修飾は、様々なタンパク質の機能に重要な役割を果たしています。特に、Notch受容体は、細胞外の領域に多様な糖修飾を受けることが知られています。Notch受容体は、細胞間のシグナル伝達に関わり、多くの発生の仕組みや疾患と関与していますが、その中で、糖鎖の異常によって引き起こされる疾患例も報告されています。Notchタンパク質の糖修飾として、O-結合型N-アセチルグルコサミン(以下、O-GlcNAc)が知られていますが、そのNotchシグナルにおける役割は明らかでなく、そのため多様な糖修飾の意義は理解されていませんでした。
Notch受容体のO-GlcNAc修飾は、糖転移酵素EOGTによって触媒されます。マウスにおいて、EOGTを欠損させると、血管内皮細胞でのNotchシグナルの低下と網膜の血管形成や血液網膜関門として知られる血管透過性の異常につながることが明らかになりました。この結果より、発生過程でNotchシグナルを適正に保つためには、O-GlcNAcを始めとした多様な糖修飾によりNotch受容体が厳密な制御を受けることが必要不可欠であることが明らかになりました。 |
ポイント
Notch受容体のN-アセチルグルコサミン修飾は、リガンド結合を制御する。
Notch受容体のN-アセチルグルコサミン修飾は、血管形成や機能に関与する。
Notchシグナルと血管発生は、糖鎖修飾により厳密な制御を受ける。
糖鎖によるタンパク質の翻訳後修飾は、糖タンパク質の機能に多様性を与えています。シグナル伝達に関わる受容体に特異的な糖修飾は、シグナル伝達経路の精密な制御に重要であり、発生過程やホメオスタシスの調節をしています。Notch受容体においては、いくつかの糖修飾が存在し、発生過程の様々な段階で重要な働きをしています。また、Notch受容体の糖修飾の異常は、先天性疾患の原因となることが知られています。Notch受容体の糖鎖修飾の1つとして、糖転移酵素EOGTによりO-GlcNAc修飾を受けるものが知られていますが、このEOGTの遺伝子変異は、アダムズ・オリバー症候群の原因とされています。アダムズ・オリバー症候群とNotchシグナル異常の関連性を示唆する報告はありましたが、EOGTとNotchシグナルにおける役割は未解明でした。そこで、本研究では、Notch受容体のO-GlcNAc修飾の生物学的意義を明らかにすることを目的としました。
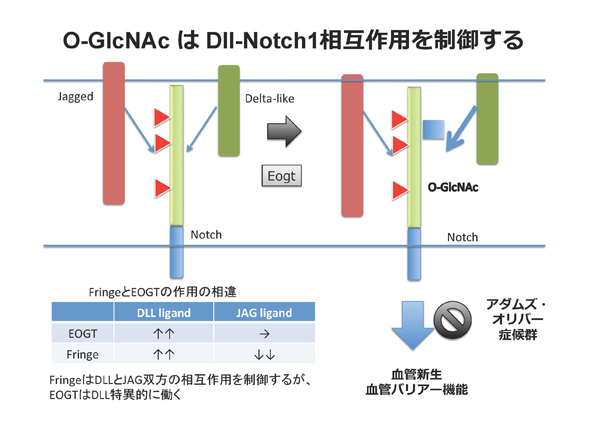
Notch受容体のリガンドとして、Delta-like(DLL)とJagged(JAG)の2種類が存在しています。それぞれのリガンドとNotch受容体の相互作用におけるEOGTの役割を明らかにするために、培養細胞を用いたリガンド結合実験を行いました。O-フコースをGlcNAc修飾するFringeと呼ばれる糖転移酵素は、DLLリガンドとの相互作用を増強するのに対して、JAGリガンドとの相互作用を阻害しました。一方、EOGTはDLLリガンドとの相互作用を増強しましたが、Jagged1リガンドを介したNotchシグナルには明らかな効果を認めませんでした。これらの結果から、EOGTはNotchとリガンドとの相互作用を新規のメカニズムで制御していることが明らかになりました。
Notchシグナルは血管形成に重要な役割を果たすことが知られています。EOGTは網膜血管の血管内皮細胞に高発現し、血管内皮におけるEOGTの欠損は、血管新生や血管バリアー機能の異常が観察されました。このような異常は、Notch1やRbpjといったNotchシグナルの構成因子の遺伝子変異によっても観察され、Eogtとの遺伝学的相互作用を示しました。また、in vitroの実験結果と一致して、Jagged1ではなくDll4の変異において見られるマウスの表現型に一致しました。
これらの結果より、発生過程でNotchシグナルを適正に保つためには、O-GlcNAcを始めとした多様な糖修飾によりNotch受容体が厳密な制御を受けることが必要不可欠であることが明らかになりました。アダムズ・オリバー症候群など、Notchシグナルの低下が原因となる先天性疾患の発症メカニズムの理解や、Notchシグナルの異常を伴う腫瘍疾患に対する治療法の開発への貢献が期待されます。
※1 Notch受容体:
Notchシグナルを伝達する受容体。4種類の受容体が知られている。細胞外ドメインに連続した上皮成長因子様ドメイン(EGFドメイン)を持ち、Notch1では36個のEGFドメインが存在し、その多くは、O-フコース、O-グルコース、O-GlcNAcといった特有の糖修飾を受ける。
※2 O-結合型N-アセチルグルコサミン(O-GlcNAc):
タンパク質のセリンもしくはスレオニン残基にO-結合でN-アセチルグルコサミンが1つ付加されている。細胞内の主要な翻訳後修飾であるが、細胞外にはNotch受容体など限られた分子にしか存在しない。
※3 アダムズ・オリバー症候群:
頭皮と頭蓋骨の欠損、四肢末端の横断型欠損を主徴とする先天性異常症であり、血管異常を伴うことが報告されている。
Shogo Sawaguchi, Shweta Varshney, Mitsutaka Ogawa, Yuta Sakaidani, Hirokazu Yagi, Kyosuke Takeshita, Toyoaki Murohara, Koichi Kato, Subha Sundaram, Pamela Stanley and Tetsuya Okajima. O-GlcNAc on NOTCH1 EGF Repeats Regulates Ligand-Induced Notch Signaling and Vascular Development in Mammals. eLife, 2017, in press (2017年4月11日の電子版に掲載)
DOI: http://dx.doi.org/10.7554/eLife.24419
研究内容
名古屋大学大学院医学系研究科
所属・職名:機能分子制御学・教授
氏名:岡島 徹也
TEL: 052-744-2068 FAX:052-744-2069
e-mail:tokajima_at_med.nagoya-u.ac.jp(_at_ は@に置き換えて下さい)
広報担当
名古屋大学医学部・医学系研究科総務課総務係
TEL:052-744-2228 FAX:052-744-2785
e-mail:iga-sous_at_adm.nagoya-u.ac.jp(_at_ は@に置き換えて下さい)