サイト内検索
分子研について
研究情報
共同利用案内
- 共同研究・施設利用案内
- 申請概要
- 共同研究受入研究室・利用装置一覧
- WEB申請
大学院
- 大学院教育
- 大学院案内
- 受験生向け情報
- 他大学の学生の受け入れ
- 在校生向け情報
お知らせ
2021/07/01
プレスリリース
・プラスチックの完全リサイクルやプラスチックによる環境汚染の解決策としてプラスチック分解酵素が注目されている
・ポリエチレンテレフタレート(PET)分解酵素を改変することにより熱安定性およびPET分解活性を大幅に向上させた
・X線結晶構造解析を用いて熱安定性向上の構造的基盤を明らかにした
・1分子観察を用いてPET分解活性向上のメカニズムを明らかにした
静岡大学の中村彰彦准教授、分子科学研究所の古賀信康准教授、飯野亮太教授らの研究チームは、世界で汎用されるプラスチックであるポリエチレンテレフタレート(PET)分解酵素のPET2を改変し、その熱安定性を6.7℃、PET分解活性を6.8倍向上させることに成功しました。また、X線結晶構造解析により熱安定性向上の構造的基盤を解明し、さらに1分子観察によりPET分解活性向上のメカニズムを解明しました。本成果は、国際学術誌ACS Catalysisに2021年6月29日付でオンライン掲載されました。
合成高分子であるプラスチックは、安価で加工が容易であるため、現代社会において大量に生産、利用されています。しかし近年、プラスチックの完全なリサイクルやプラスチックによる環境汚染の浄化が、持続的社会の実現の観点で世界的課題となっています。特に、ポリエチレンテレフタレート(PET)は生産量が多く、飲料用ボトルや衣料品、包装材などに広く使用されています。PETは、物理的にも化学的にも安定した結晶性構造を形成するため、環境中に長く留まることが報告されています。
高い安定性を有するPETの高分子鎖は、テレフタル酸とエチレングリコールのエステルで構成されています。そのためエステル分解酵素の一部は、その鎖を切断してPETを分解する能力を持っています。PETを分解すると報告されている酵素の一つは、植物のクチクラ層(ワックス層)の分解酵素として知られているクチナーゼです。クチナーゼを改変した非天然型酵素は現在、酵素によるPET分解の実用化において最も有望と言われています。また2016年には、PETを炭素源として生育可能な細菌Ideonella sakaiensis 201-F6が日本で発見され、この細菌がPET分解酵素IsPETaseを産生することが明らかとなり大きな話題となりました。さらに最近、高温の人工施設で採取されたメタゲノムライブラリー(*1)から発見された耐熱性酵素がPETを分解することが明らかにされ、PET2と名付けられました。PETは70℃付近にガラス転移温度(*2)を持つため、70℃より高温で反応を行えると分解の効率が大きく向上すると期待されており、PET分解酵素の熱安定のさらなる改善が求められています。PET2は、耐熱性PET分解酵素の候補の一つです。本研究では、PET2の改変を行い、その熱安定性とPET分解活性を大幅に向上させることに成功しました(図)。
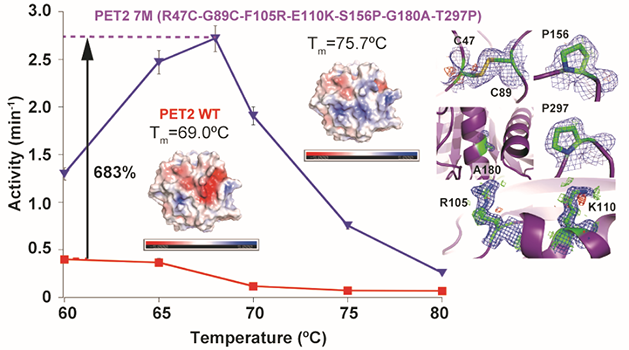
図.PET分解酵素PET2を改変し熱安定性を6.7℃、PET分解活性を6.8倍向上させた。Tmは変性温度、構造図の色分けは表面の電荷(青:正、赤:負)を表す。
まず、天然型PET2の熱安定性を調べました。円偏光二色性(*3)の測定で、変性温度が69.0℃であることが明らかとなりました。また、高分子固体であるPETの単位構造の一部を構成する水溶性のBHET(bis(2-hydroxyethyl) terephthalate)をモデル基質として用い、70℃、1時間の熱処理で天然型PET2の活性が完全に消失することを明らかとしました。
次に、アミノ酸変異の導入により熱安定性と活性の向上を試みました。ホモロジーモデリング(*4)で得られたPET2の立体構造モデルに基づいて、プロリン変異の導入によるループ構造の安定化、アラニン変異の導入による触媒部位近傍のヘリックス構造の安定化、およびジスルフィド結合(*5)の導入による全体構造の安定化を試みました。また、IsPETaseが特徴的に持つ正電荷アミノ酸残基を、PET2の表面に導入しました。個々のアミノ酸残基(ジスルフィド結合の場合は2つのシステイン残基のペア)の変異をまずは別々に試し、次に熱安定性とPET分解活性が向上した変異の組み合わせを試しました。その結果、7ヵ所に変異を入れたPET2 7Mを得ることに成功しました。PET2 7Mの変性温度は75.7℃で、天然型PET2よりも6.7℃の向上がみられました。
続いて、PET2 7M のPET分解活性を天然型と比較しました。60℃におけるPET2 7M のPET分解活性は、天然型PET2よりも3.3倍向上していました。また、PET分解の至適温度は天然型PET2の60℃から68℃に8℃向上し、それぞれの至適温度でのPET分解活性は天然型PET2の6.8倍に達しました。さらに、PET2 7Mは少なくとも24時間、至適温度の68℃で変性することなく安定にPETを分解し続けることも確認されました。
また、熱安定化の構造的基盤を検証しました。PET2 7Mの立体構造をX線結晶構造解析により決定し、プロリン変異導入によりループ構造は変化せず安定化されていること、アラニン変異の導入により触媒部位近傍のヘリックス構造が安定化されていること、およびジスルフィド結合が確かに形成されていることが確認されました。また、導入した正電荷アミノ酸残基により、PET2 7Mの表面が正電荷を持つことも確認されました。
さらに、1分子観察を用いて分解活性向上のメカニズムを検証しました。PET2 7Mと天然型PET2に蛍光色素を導入し、酵素分子のPET表面への結合と解離を1分子観察しました。その結果、PET2 7Mは天然型PET2に比べ、PET表面へ結合する速さが3.4倍であることが明らかとなりました。この差は、同じ温度(60℃)で比較したPET2 7Mと天然型PET2のPET分解活性の差(3.3倍)とほぼ同じでした。他方、PETに結合してから解離するまでの時間(解離の速さ)は、PET2 7Mと天然型PET2で違いはありませんでした。これらの結果と構造解析の結果から、表面に正電荷を持つPET2 7MはPET表面への結合が速いため、天然型よりも高いPET分解活性を示すことが明らかとなりました。
プラスチックの完全なリサイクルやプラスチックで汚染された環境の浄化は、持続的社会を実現する上で重要な課題です。本研究により、PETを分解する耐熱性酵素に新たなメンバーが加わりました。また、PET分解酵素の高活性化には、PET表面への結合の速さが重要であることが明らかとなりました。今後は、本研究で得られたPET分解酵素をさらに改変して耐熱性をさらに向上させることで、PETのガラス転移温度(70℃)以上でPET分解反応を行えるようにしたいと考えています。これにより、PET分解の効率がさらに改善されると期待されます。
*1)メタゲノムライブラリー:
環境から直接回収された染色体DNAのライブラリー(試料)。その環境に棲む多様な微生物由来の染色体DNAを含む。
*2)ガラス転移温度:
PET等の樹脂が固い固体(ガラス)状態から柔らかいゴム状態に変化する温度。
*3)円偏光二色性:
物質が円偏光を吸収する際に左円偏光と右円偏光に対して吸光度に差が生じる現象のこと。タンパク質の立体構造を大まかに調べることができる。
*4)ホモロジーモデリング:
立体構造が既に分かっているタンパク質の中からアミノ酸配列が似ているものを探し、それをもとに立体構造のモデルを作る手法。
*5)ジスルフィド結合:
2つのチオールが形成する共有結合。タンパク質ではシステイン残基がチオールを持ち、近傍に存在する2つのシステイン残基間で形成される。
掲載誌:ACS Catalysis
論文タイトル: “Positive charge introduction on the surface of thermostabilized PET hydrolase facilitates PET binding and degradation”
(熱安定化したPET分解酵素表面への正電荷の導入によりPETへの結合と分解が促進される)
著者: Akihiko Nakamura, Naoya Kobayashi, Nobuyasu Koga, Ryota Iino
掲載日:2021年6月29日(オンライン公開)
DOI:10.1021/acscatal.1c01204
中村彰彦 准教授(静岡大学)
小林直也 研究員(生命創成探究センター、当時)
古賀信康 准教授(生命創成探究センター/分子科学研究所)
飯野亮太 教授(分子科学研究所)
文部科学省 卓越研究員事業
科研費・新学術「発動分子科学」 JP18H05424
科研費・基盤研究(B)18H02418
科研費・新学術(公募)18H04755
住友財団・環境研究助成 193039
ExCELLS特別共同研究
中村彰彦
静岡大学 農学部 テニュアトラック准教授
TEL: 054-238-4869
E-mail: nakamura.akihiko_at_shizuoka.ac.jp
飯野亮太
分子科学研究所 教授
TEL: 0564-59-5230
E-mail: iino_at_ims.ac.jp
静岡大学 広報室
TEL: 054-238-5179
E-mail: koho_all_at_adb.shizuoka.ac.jp
自然科学研究機構 分子科学研究所 研究力強化戦略室 広報担当
TEL: 0564-55-7209 FAX: 0564-55-7374
E-mail: press_at_ims.ac.jp
※_at_は@に変換してください。