サイト内検索
分子研について
研究情報
共同利用案内
- 共同研究・施設利用案内
- 申請概要
- 共同研究受入研究室・利用装置一覧
- WEB申請
大学院
- 大学院教育
- 大学院案内
- 受験生向け情報
- 他大学の学生の受け入れ
- 在校生向け情報
お知らせ
2023/04/04
プレスリリース
岡山大学学術研究院医歯薬学域(薬)の山下敦子教授、自然科学研究機構・分子科学研究所の岡崎圭一准教授、京都大学大学院医学研究科の島村達郎特定准教授、理化学研究所放射光科学研究センターの平井照久チームリーダー(研究当時)らの研究グループは、尿路結石形成に関わるシュウ酸分解菌が腸内からシュウ酸を吸収するときに利用するシュウ酸輸送体の立体構造を、SPring-8を用いて解明しました。
これらの研究成果は4月3日、英国の科学雑誌「Nature Communications」に掲載されました。
尿路結石症は、3大激痛の1つとも言われ、日々の食事でホウレンソウなどの食品から摂取したシュウ酸が、尿路でカルシウムなどと結晶化して結石を生じることで起こります。腸内細菌の1種であるシュウ酸分解菌は、腸内のシュウ酸を吸収・分解することで、この結石形成リスクを下げています。研究グループは、シュウ酸を分解菌内へ吸収する役目を担うシュウ酸輸送体の立体構造を解明し、この分子が、シュウ酸に似た他の栄養素とシュウ酸を厳密に見分け、シュウ酸だけを結合しその構造を変化させることで、効率よく菌内に運ぶ仕組みを明らかにしました。
尿路結石症を防ぐ方法の1つとして、シュウ酸分解菌の治療応用の可能性が検討されています。本研究で得られた知見は、同菌に着目した治療法開発の基盤情報となることが期待できます。
たくさんの研究者と学生さんの協力により、私たちの腸内で起こっている反応の一端が少しずつ見えてきました。この研究はいま患者さんの痛みを和らげることはできませんが、将来痛みに苦しむ患者さんを減らせる一助となりますように。(山下)
私たちは、日々の食事を通して、野菜・お茶・ナッツ類などの食品から、シュウ酸を摂取しています。一方、体内のシュウ酸量が過剰となると、血中に含まれるカルシウムと不溶性の塩を形成し、尿路結石の原因となります。この尿路結石は、3大激痛の1つとも言われる激しい痛みを引き起こします。
私たちの腸内には腸内細菌と呼ばれる多種多様な細菌が共生していますが、このうちの1種であるシュウ酸分解菌O. formigenesは、上述した私たちのシュウ酸代謝と深い関わりを持ちます。この菌は、腸内のシュウ酸を唯一の炭素源として吸収し、その分解によってエネルギーを得て生息しています。かたや私たちにとっては、このシュウ酸分解菌のはたらきのおかげで尿路結石形成のリスクが減少しており、シュウ酸分解菌とはwin-winの関係を結んでいると言えます。実際、何らかの事情で腸内に同菌がいないか少ない人は、尿路結石形成のリスクが高いことが知られています。
シュウ酸分解菌O. formigenesに存在するシュウ酸輸送体OxlTは、この過程の鍵とも言える、シュウ酸の菌体内への吸収と、その分解産物であるギ酸の菌体外への排出を担っています。この過程は、私たちが食品から摂取し、消化された多種多様な物質が流れている腸内環境下で起こりますが、OxlTがどのようにしてその中からシュウ酸だけを見分けて菌体内に取り込んでいるのか、詳しいメカニズムはわかっていませんでした。
研究グループは、大型放射光施設・SPring-8(兵庫県佐用町)を用いて、X線結晶構造解析によりOxlTの立体構造を解明しました。異なる条件下で得られた2種類の結晶を解析した結果、1つはシュウ酸の輸送経路を菌体の外(腸内側)に開いた「外開き構造」、1つはシュウ酸を結合し輸送経路を閉じている「閉じ構造」という、OxlTが輸送の各段階でとる構造のうちの2段階の構造がわかりました。OxlTは、「外開き構造」では、正電荷を帯びた輸送経路を開いており、シュウ酸が結合しない限り電荷反発で経路を閉じられない一方、負電荷を帯びたシュウ酸が結合すると、電荷が中和され輸送経路を閉じて次の段階である「閉じ構造」に移行できる仕組みとなっていました。また、「閉じ構造」では、OxlT分子の中心に基質結合ポケットが形成され、その中にシュウ酸を結合している様子が明らかになりました。シュウ酸はカルボキシ基を2つ持つジカルボン酸ですが、クエン酸回路の代謝産物の1つであるコハク酸をはじめとする様々なジカルボン酸は、腸内を流れる栄養素の中にも、シュウ酸分解菌内にも存在します。一方、OxlT内の結合ポケットは、炭素数2の最小のジカルボン酸であるシュウ酸であれば収まることができ、炭素数4のコハク酸などシュウ酸よりも大きいジカルボン酸は、大きすぎて収まらないことがわかりました。このことにより、私たちや分解菌にとって栄養素となるシュウ酸以外のジカルボン酸については、誤って菌内に取り込んだり菌内から排出したりしない仕組みとなっていました。
今回のOxlTの2種類の構造で見られたように、一般的に輸送体タンパク質は、構造を変えながら物質を細胞の外から中へ輸送します。OxlT分子は、構成アミノ酸の約8分の1を柔軟性が高いグリシンが占めており、構造変化が起こりやすい柔軟な構造を持っていることがわかりました。また、その変化をコンピュータシミュレーションした結果、輸送経路を閉じているたった1つのアミノ酸が向きを変えると、掛け金が外れたように輸送経路を開き、「閉じ構造」から「外開き構造」に転換することがわかりました。このような構造変化の起きやすい構造的特徴が、OxlTによる効率のよいシュウ酸吸収とギ酸排出を支えているものと考えられます。
今回OxlTによるシュウ酸輸送の最初の2段階の構造が初めて明らかになりました。現在、尿路結石発症原因となる高シュウ酸尿症改善法の1つとして、シュウ酸分解菌の経口投与が検討されています。本研究で得られる知見は、シュウ酸吸収条件の最適化など、同菌に着目した治療法開発の基盤となることが期待できます。
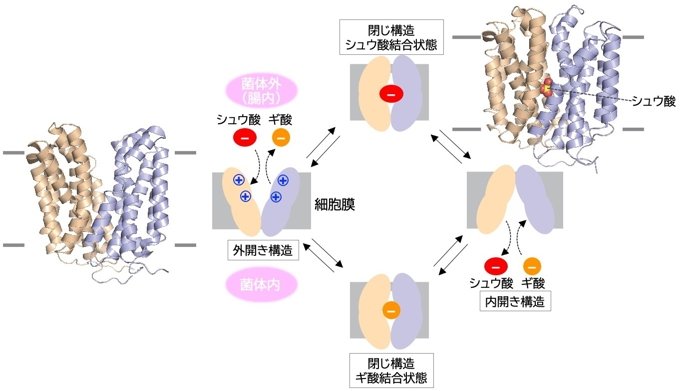
図.OxlTによるシュウ酸輸送過程と今回明らかになった結晶構造
論文名:Structure and mechanism of oxalate transporter OxlT in an oxalate-degrading bacterium in the gut microbiota
掲載紙:Nature Communications
著者:Titouan Jaunet-Lahary, Tatsuro Shimamura, Masahiro Hayashi, Norimichi Nomura, Kouta Hirasawa, Tetsuya Shimizu, Masao Yamashita, Naotaka Tsutsumi, Yuta Suehiro, Keiichi Kojima, Yuki Sudo, Takashi Tamura, Hiroko Iwanari, Takao Hamakubo, So Iwata, Kei-ichi Okazaki, Teruhisa Hirai, Atsuko Yamashita
DOI:10.1038/s41467-023-36883-5
URL:https://www.nature.com/articles/s41467-023-36883-5
本研究は、日本学術振興会・科学研究費補助金(JP20H03195, JP18H02415, JP26440086)、公益財団法人小柳財団、公益財団法人武田科学振興財団、国立研究開発法人日本医療研究開発機構・創薬等先端技術支援基盤プラットフォーム事業(JP20am0101079)の支援を受けて実施しました。
岡山大学学術研究院医歯薬域(薬)
教授 山下 敦子
TEL: 086-251-7974
FAX: 086-251-7974
E-mail: a_yama_at_okayama-u.ac.jp
自然科学研究機構 分子科学研究所
准教授 岡崎 圭一
TEL: 0564-55-7468
E-mail: keokazaki_at_ims.ac.jp
京都大学大学院医学研究科
特定准教授 島村 達郎
TEL: 075-753-4389
E-mail: t.shimamura_at_mfour.med.kyoto-u.ac.jp
理化学研究所放射光科学研究センター
チームリーダー(当時) 平井 照久
E-mail: teruhisahirai_at_gmail.com
※ _at_は@に変換してください。