サイト内検索
分子研について
研究情報
共同利用案内
- 共同研究・施設利用案内
- 申請概要
- 共同研究受入研究室・利用装置一覧
- WEB申請
大学院
- 大学院教育
- 大学院案内
- 受験生向け情報
- 他大学の学生の受け入れ
- 在校生向け情報
お知らせ
2025/05/02
プレスリリース
東京科学大学(Science Tokyo)総合研究院 化学生命科学研究所の澤田知久准教授と東京大学の藤田誠卓越教授(兼 分子科学研究所 卓越教授)、お茶の水女子大学の下川航也教授らの研究チームは、ペプチド(用語1)を金属イオンと自己組織化(用語2)させることによって、正十二面体リンク(用語3)の幾何構造を持つ球殻分子構造の構築に初めて成功しました。
ウイルスキャプシド(用語4)などに見られる球殻分子構造は、分子を内包し運搬できる機能をもちます。本研究グループは、幾何学に基づく構造予測と化学合成により、その人工構築を目指してきました。これまでに、短いペプチドが金属イオンとの自己組織化によって絡まり合いながら多面体状に集合する性質を発見し、正四面体リンクや立方体リンクの分子構造の構築に成功しています。しかし、さらに高度な正十二面体リンクの構築は未達成でした。
今回の研究では新たに、ペプチド配列に配位性側鎖(用語5)を1つ導入することで、正十二面体リンクの構築に成功しました。X線結晶構造解析(用語6)によって、その構造は外径6.3ナノメートルの巨大球殻分子構造であり、60の交点数(用語7)を持つ複雑な絡まりに基づくことを明らかにしました。さらに、球殻構造を構成する60個の金属イオンの配置は切頂二十面体(用語8)であり、ウイルスキャプシドに見られるゴールドバーグ多面体(用語9)の特徴も併せ持つことが分かりました。このような「絡まり方」と「多面体」という2つの幾何学的要素に基づいた構造予測により、さまざまなウイルスキャプシド状構造の人工構築が可能になると期待できます。
本研究は、東京科学大学の澤田知久准教授、東京大学の藤田誠卓越教授(兼 分子科学研究所 卓越教授)、猪俣祐貴大学院生(当時、東京大学博士課程学生)、小熊蒼汰大学院生(当時、東京大学博士課程学生)、佐柄直大学院生(当時、東京科学大修士課程学生)、お茶の水女子大学の下川航也教授らによって行われ、「Chem」(Cell姉妹誌)のオンライン版(現地時間5月1日付け、オープンアクセス)に掲載されます。
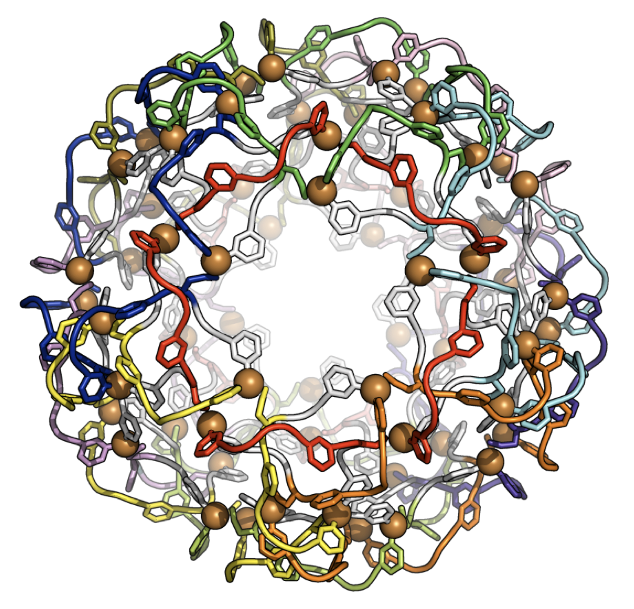
構築に成功した正十二面体リンクの球殻分子構造
球状ウイルスキャプシドやタンパク質集合体に見られる球殻分子構造は、外部の環境から隔離されたナノサイズの空間を内部に持つことから、小分子の運搬や貯蔵、反応などの重要な機能が発現することが知られています。これまで、天然のウイルスキャプシドや生物の作り出すタンパク質を人工改変することによって、球殻構造へ集合させた例は存在しますが、化学合成によってペプチドからなる球殻分子構造を一から精密に構築することは困難でした。その理由は、安定な立体構造を持つタンパク質と異なり、構造が定まらない柔軟な短いペプチドは無秩序に会合しやすいためです。
研究チームはこれまでに、ペプチド配位子(用語10)が金属イオンと結合して自己組織化する際に、多重に絡まり合う性質があることを見いだし、秩序ある構造の正四面体リンクや立方体リンクの精密構築に成功してきました(図1A、B)。さらに高度な正十二面体リンク(図1C)は、立方体リンクよりも球形に近づくため、ウイルスキャプシドのような球殻分子構造になると考えられますが、その絡まりの複雑さのために設計指針がなく、構築が困難でした。
正十二面体リンクの精密構築方法を開発できれば、巨大な球殻分子構造の人工ウイルスキャプシド構造を自在に化学合成できるようになり、さまざまな機能性分子材料の創製に応用できると考えられます。また、それは60の交点数を持つ前例のない複雑な絡まりを精密化学合成することを意味し、合成学における挑戦的な到達目標となっていました。
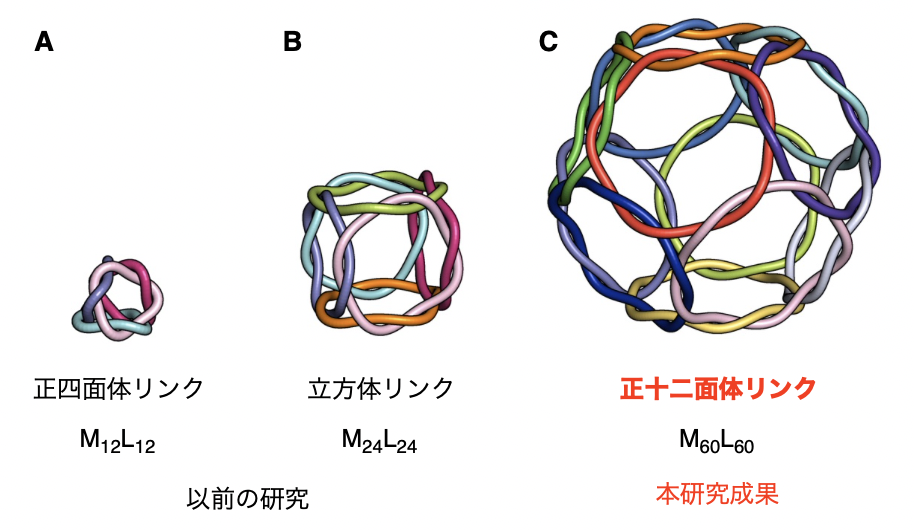
図1 ペプチド配位子と金属イオンの自己組織化で得られる多面体リンク系列
(A:四面体リンクM12L12、B:立方体リンクM24L24、C:十二面体リンクM60L60)
本研究では、ペプチド配列に配位性側鎖を新たに導入することを検討しました。以前の研究では、5残基からなるペプチドP-P-X-A-P配列(P:プロリン、X:人工アミノ酸、A:アラニン)を溶液中で銀イオンと混合すると、立方体リンクの集合構造M24L24(M:金属イオン、L:ペプチド配位子)が得られることを明らかにしました(図2A)。この場合には、ペプチド配列の両末端に金属イオンと結合する部位を導入した、二官能性(用語11)のペプチド配位子となっており、二配位(用語12)の銀イオンと結合することで、銀―ペプチド―銀―ペプチド―......と交互に連なり、リング構造になります。そのリングが6つ、立方体状に自発的に絡まり合うことで立方体リンクM24L24が形成されました。一方で今回は、ペプチド配列中のAを金属配位性の残基(Pra:プロパルギルグリシン)へ置き換えて三官能性のペプチド配位子とし、用いる金属イオンを銀イオンから三配位の銅(I)イオンに変更しました(図2B)。この設計変更によって、ペプチド鎖同士の絡まり方が大きく変化した結果、正十二面体リンクの集合構造M60L60が得られることが明らかになりました。
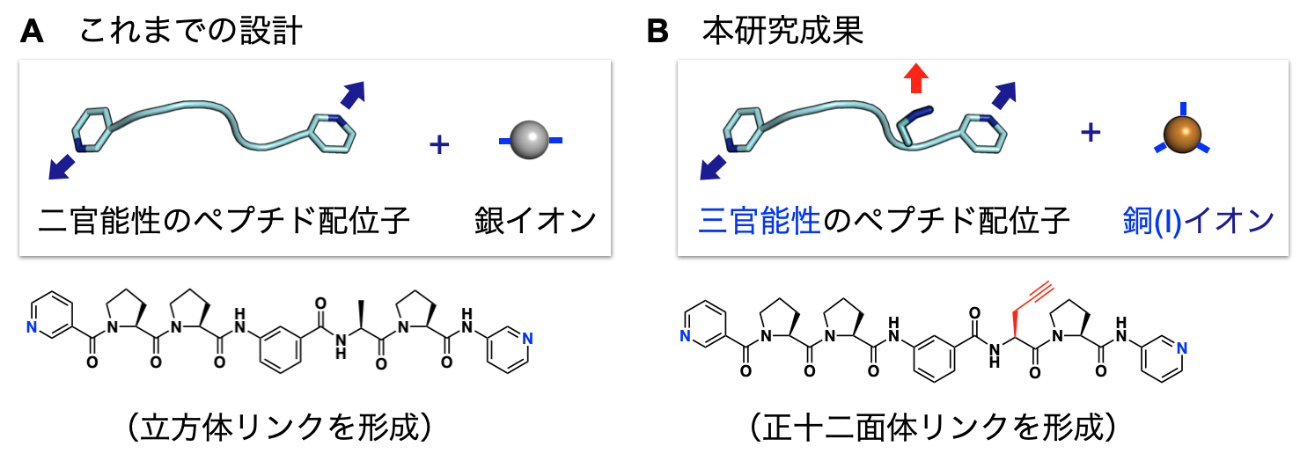
図2 分子設計
(A:以前の設計、B:今回の設計)
こうした分子設計に基づいて、実際にP-P-X-Pra-P配列のペプチドと銅(I)イオンを溶液中で混合し、自己組織化によってこの溶液から得られた単結晶をX線結晶構造解析により調べたところ、外径6.3ナノメートルの球殻構造が原子分解能で観測されました(図3A、B)。その構造は、60個の銅(I)イオンと60個のペプチド配位子の計120個の成分からなる精密な集合体M60L60であることが分かりました。その構造において、銅(I)イオンを起点としてそこに結合したペプチド配位子のN末端を経てPra残基に結合した銅(I)イオンへたどっていくと、五角形のリング構造が浮かび上がります(図4A)。構造中にはそのようなリングが12個存在し、互いに絡まり合って十二面体リンクの幾何構造となっています。60の交点数を持つこの多面体絡まりは、以前の研究で得られた四面体リンクや立方体リンクから存在を予測し、到達目標としていたものでした。得られた集合体M60L60では、この多重の絡まりによって骨格に堅牢(けんろう)性が備わり、内部に4ナノメートル径の巨大なナノ空間が形成していることも分かりました(図3C)。
またこのX線結晶構造解析では、このM60L60構造が別の幾何構造としての特徴を併せ持つことも見いだしました。この構造において、ペプチド配位子のN末端からC末端へ主鎖をたどっていくと、三つ葉結び目(用語13)が単位構造として浮かび上がり、これが20個集合し、切頂二十面体となっています(図4B)。20枚ある六角形の面はこの三つ葉結び目構造であり、12枚ある五角形の面は空洞となっています。これは、六角形と五角形の面を張り合わせてできるゴールドバーグ多面体の一種であり、天然のウイルスキャプシドに見られる幾何学的特徴です。六角形と五角形の面の張り合わせ方の違いによって、多面体の拡張が可能であり、本系はさらに大きな球殻分子構造が将来的に構築可能であることを示唆しています。
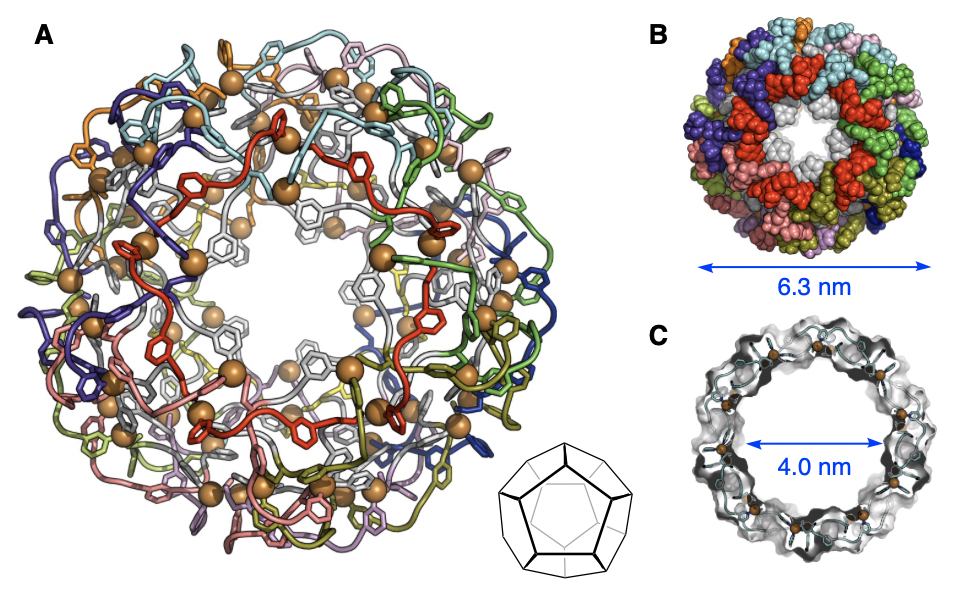
図3 M60L60の結晶構造
(A:針金/ループによる表示、B:実体積表示、C:断面図)
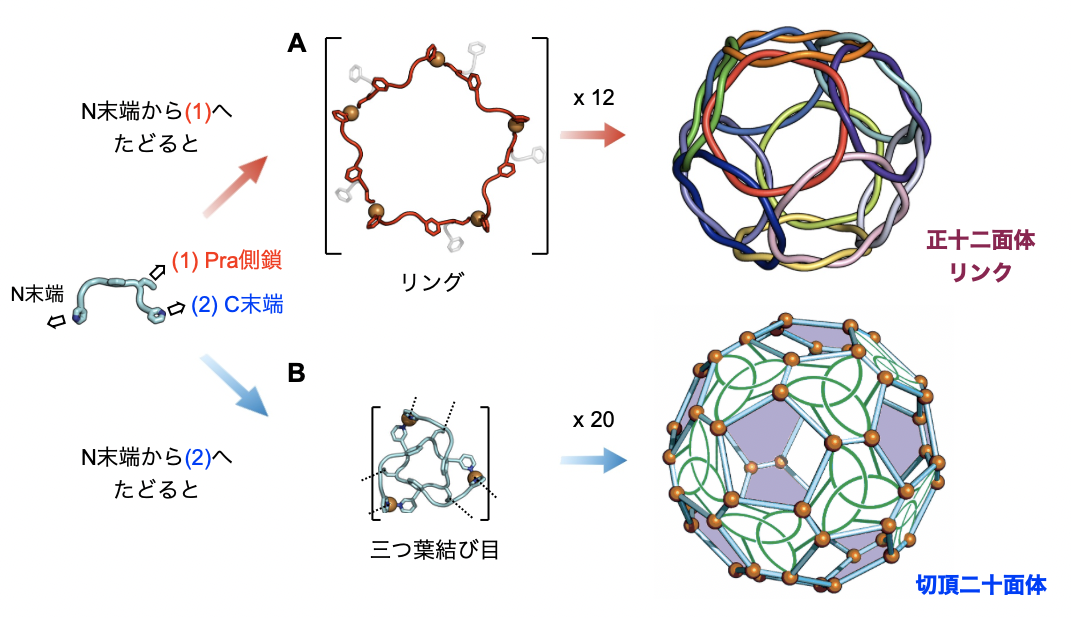
図4 M60L60の二種類の幾何学的特徴
(A:正十二面体リンク、B:切頂二十面体)
本研究ではさらに、自己組織化を行った溶液を分析することにより、M60L60構造が単一の生成物であることも明らかにしました。ペプチド配位子と銅(I)イオンの1:1混合溶液に対してSAXS測定(用語14)を行ったところ、直径約6.7 ナノメートルの粒子の存在が確認され、これは上述の結晶構造解析で確認された球殻構造の直径と良い一致を示しました(図5A)。またNMR測定(用語15)でも、同じ溶液から高対称性構造を示す信号が検出され、M60L60構造だけが生成したことを確認しました(図5B)。一般に、銅(I)イオンからなる金属タンパク質や錯体は容易に空気酸化されて変性・分解することが知られていますが、M60L60構造は大気下で十分に安定であり、別の構造への変化は見られませんでした。これは、Pra残基と銅(I)イオンの結合によって特異的に安定化されているためと考えられます。
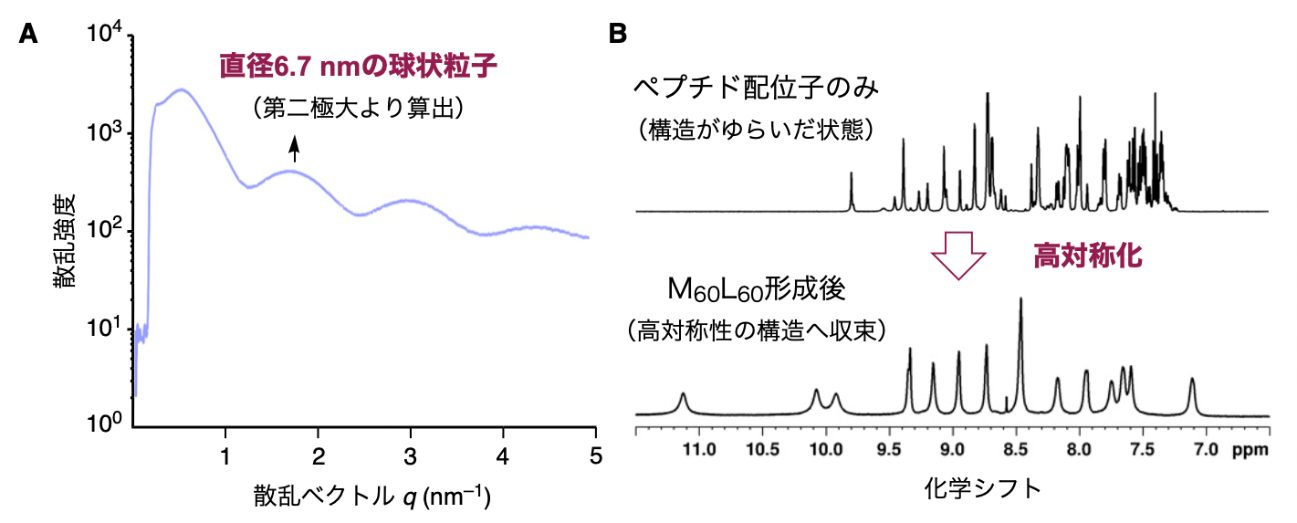
図5 溶液中におけるM60L60球殻構造の構造解析
(A:SAXS測定、B:NMR測定)
図6 外面化学修飾したM60L60構造
(紫色:M60L60骨格、黄色:60本のDEG基)
このようにして生成されたM60L60構造は、化学修飾が可能であることも実証しました。ジエチレングリコール基(DEG基)をあらかじめ導入したペプチド配位子を、銅(I)イオンと混合することで、M60L60構造の外表面に60本のDEG基を精密修飾できることを確認しました(図6)。これにより、各種有機溶媒への溶解性の向上が確認されるとともに、今後さまざまな官能基修飾が可能であることも示しています。
わずか5残基のペプチド配列と金属イオンを混ぜ合わせるだけで、6ナノメートルを超える巨大な球殻分子構造が精密構築できるという事実は、生体高分子が作り出す緻密なナノ構造を高効率に人工合成できることを示しています。得られた中空構造は、高分子やナノマテリアルといった巨大分子の内包や運搬、反応場としての利用が期待されます。また本研究成果は、分子の自己組織化において、分子鎖の絡まり方と多面体という2つの幾何学に基づく構造予測や解析の重要性を示しています。
本研究成果により、幾何学的な考察と実験的な試行錯誤を双方向で実施することで、絡まりを持つ多面体構造を拡張できることが分かりました。今回正十二面体リンクを得たことで、多面体絡まりの系列における最終到達目標を達成したと当初は考えられました。しかし、構造を多面体として捉え直すと最小のゴールドバーグ多面体に相当することから、さらに大きな球殻構造への拡張が可能です。今後は、より巨大で、より大きい交点数を持つ球殻分子構造の精密構築を進め、生体系で見られるウイルスキャプシドと遜色ない巨大球殻構造の構築を目指していきます。また、得られたM60L60球殻構造をプラットフォームとして、さまざまな官能基修飾による機能化や内部空間への分子の内包や運搬への利用も進めたいと考えています。
本研究は、科学技術振興機構(JST)戦略的創造研究推進事業 さきがけ(課題番号:JPMJPR20A7)、日本学術振興会(JSPS)科学研究費助成事業(課題番号:JP19H05461、JP24K01465)などの支援により実施されました。
掲載誌:Chem
論文タイトル:An M60L60 metal-peptide capsid with a 60-crossing woven network
著者:Yuuki Inomata, Sota Oguma, Nao Sagara, Ami Nishijima, Yuta Saburomaru, Satoshi Yoshida, Takashi Kajitani, Koya Shimokawa, Sota Sato, Michito Yoshizawa, Makoto Fujita,* and Tomohisa Sawada*
DOI:10.1016/j.chempr.2025.102555
澤田 知久(サワダ トモヒサ) Tomohisa SAWADA
東京科学大学 総合研究院 化学生命科学研究所 准教授
研究分野:超分子化学
(研究に関すること)
東京科学大学 総合研究院 化学生命科学研究所 准教授
澤田 知久
Email: sawada.t.ak_at_m.titech.ac.jp(_at_は@に変換してください。)
TEL: 045-924-5230
藤田 誠(フジタ マコト) Makoto FUJITA
東京大学 国際高等研究所 東京カレッジ 卓越教授
(兼:自然科学研究機構 分子科学研究所 卓越教授)
Email: mfujita_at_appchem.t.u-tokyo.ac.jp(_at_は@に変換してください。)
TEL: 04-7131-0801
(報道取材申し込み先)
東京科学大学 総務企画部 広報課
Email: media_at_ml.tmd.ac.jp(_at_は@に変換してください。)
TEL: 03-5734-2975 FAX: 03-5734-3661
自然科学研究機構 分子科学研究所 研究力強化戦略室 広報担当
Email: press_at_ims.ac.jp(_at_は@に変換してください。)
TEL: 0564-55-7209
お茶の水女子大学 広報・ダイバーシティ推進課
Email: info_at_cc.ocha.ac.jp(_at_は@に変換してください。)
TEL: 03-5978-5105
科学技術振興機構 広報課
Email: jstkoho_at_jst.go.jp(_at_は@に変換してください。)
TEL: 03-5214-8404 FAX: 03-5214-8432
(JST事業に関すること)
科学技術振興機構 戦略研究推進部 グリーンイノベーショングループ
安藤 裕輔(アンドウ ユウスケ)
E-mail:presto_at_jst.go.jp(_at_は@に変換してください。)
TEL: 03-3512-3526 FAX: 03-3222-2066