サイト内検索
分子研について
研究情報
共同利用案内
- 共同研究・施設利用案内
- 申請概要
- 共同研究受入研究室・利用装置一覧
- WEB申請
大学院
- 大学院教育
- 大学院案内
- 受験生向け情報
- 他大学の学生の受け入れ
- 在校生向け情報
お知らせ
2025/12/10
プレスリリース
分子科学研究所のMd. Iqbal Mahmood博士研究員、岡崎圭一准教授(岡崎准教授は総合研究大学院大学を併任)らの研究グループは、細胞内でGTP(1)加水分解エネルギーを使って膜を絞って切り離すタンパク質「ダイナミン(Dynamin)」の動作原理を解明することに成功しました。本研究では、粗視化分子動力学シミュレーション(2)という手法を用いて、ダイナミン集合体と脂質膜が相互作用するシミュレーション系を構築し、GTP→GDP状態における構造変化と膜狭窄との化学力学共役機構を調べました。シミュレーション結果から、ダイナミン集合体が形成するリングがGDP状態へ移行後に"ゆるむ"変化を起こし、被覆されていない膜領域において間接的に膜チューブを細くする力を誘起するという新たなメカニズムを提案しました。この成果は、細胞膜リモデリングに関わる分子機構の解明に大きく寄与するとともに、将来的には細胞内輸送機構の制御や人工ナノデバイス設計の応用への道を拓くものです。
本研究成果は、国際学術誌『The Journal of Physical Chemistry Letters』に、2025年11月20日付でオンライン掲載されました。
細胞における内在化やエンドサイトーシス(3)の過程では、細胞膜が陥没して形成されたチューブ状ネック領域が狭まり、最終的に切断されて小胞化が起こります。この膜切断の際、ダイナミンというGTP加水分解酵素が、膜チューブにリング状に集合し、GTP加水分解エネルギーを使って構造変化を起こし、膜を物理的に狭窄・切断すると考えられています(図1)。ただし、その一連の過程、特に「GTP状態からGDP状態へ移行する際のダイナミン集合体リングの構造変化がどのように膜狭窄に寄与するか」は、実験的には観察が難しく、分子レベルの理解が不足していました。
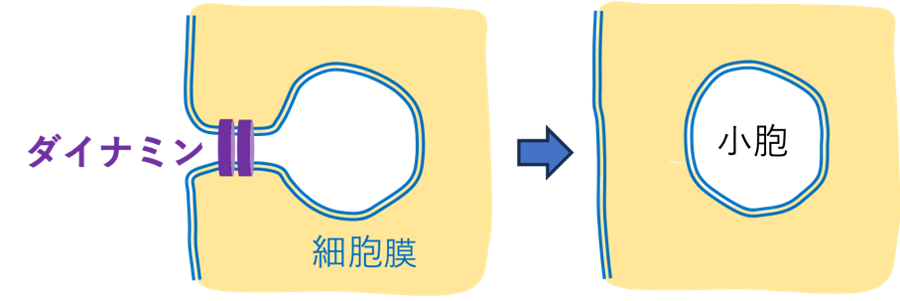
図1.エンドサイトーシス過程におけるダイナミンによる細胞膜切断
本研究では、ダイナミンが、どのように細胞膜チューブを細くし、最終的に切り離すのかという仕組みを、コンピュータによる大規模シミュレーションを用いて調べました。ダイナミンはエネルギー源であるGTPを使って形を変えることが知られていますが、その形の変化と膜の狭窄がどのように結びついているのかは、これまでの実験だけでは十分に説明できていませんでした。
今回、粗視化分子動力学手法を活用することで、現実に近い大きさのダイナミン集合体と膜チューブを同時に扱えるシミュレーション環境を構築し(図2)、ダイナミンがGTP状態からGDP状態へと変化するときの動きを詳細に再現しました。その結果、ダイナミンは単に膜を「ぎゅっと締め付ける」のではなく、むしろGTP加水分解後に構造が"ゆるむ"ことで、周囲の膜チューブが細くなるという新しいメカニズムが見えてきました(図3)。この発見により、タンパク質の動きと細胞膜の変形がどのように連動して小胞が形成されるのかを、これまでにない視点で説明することができます。
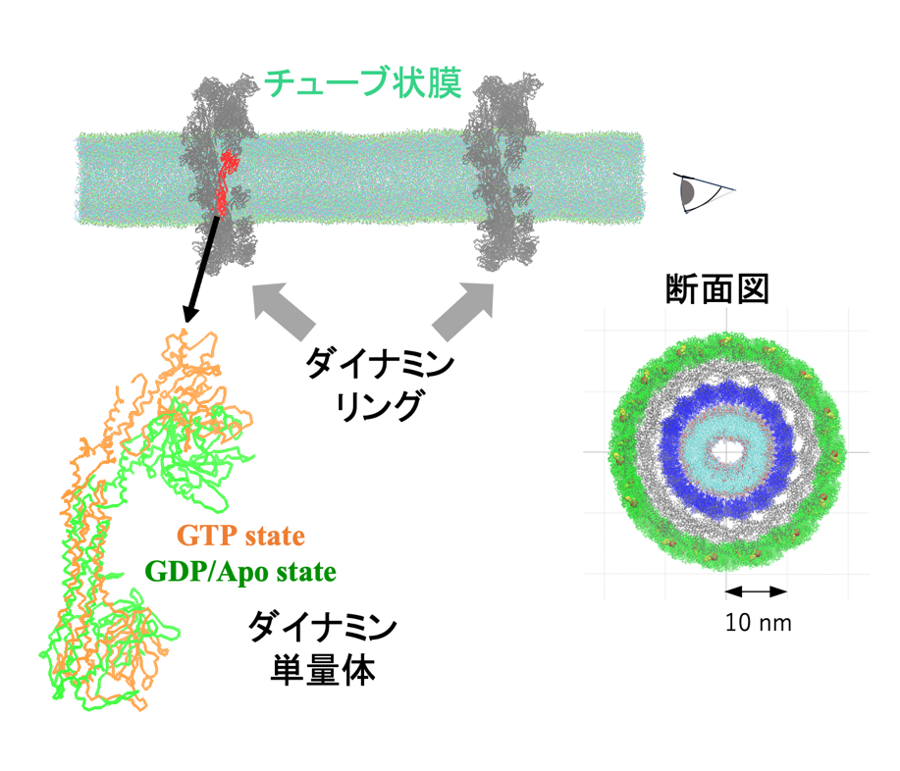
図2.粗視化分子シミュレーションのセットアップ
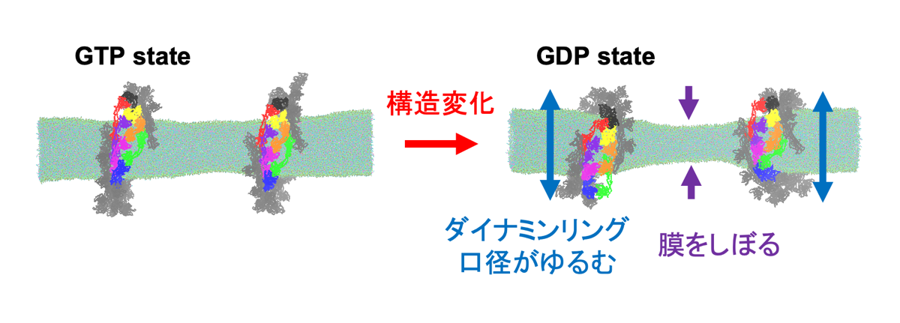
図3.ダイナミンリングが"ゆるむ"ことで、周囲の膜をしぼる
図4.ダイナミンリングの構造変化が周囲の膜をしぼる様子
(図をクリックすると動画が再生されます)
本研究で、タンパク質の構造変化と膜が複雑に関わり合う現象をコンピュータ上で再現できるようになったことで、今後は細胞内輸送やウイルス侵入など、さまざまな生命現象の理解が一層進むことが期待されます。また、この知見は、細胞の膜変形を応用した人工ナノデバイスの開発や、膜の働きに異常が生じる病気の研究にも応用できる可能性があります。
(1) GTP(グアノシン三リン酸)
細胞内でエネルギーの貯蔵や受け渡しに使われる分子の一種。リン酸を三つ持つ状態が GTP、二つ持つ状態が GDP を指す。GTP が加水分解されて GDP とリン酸に変化するときにエネルギーが放出され、ダイナミンなどのタンパク質の構造変化を通じて膜を変形させる原動力となる。
(2) 粗視化分子動力学シミュレーション
複数の原子をまとめた粒子で表現する粗視化分子モデルを用いて、分子の動きをシミュレーションする計算手法のこと。大規模分子系のシミュレーションを効率的に行うことができる。
(3) エンドサイトーシス
細胞が外部の物質や情報を取り込むときに働く仕組みの一つのこと。細胞膜の一部が内側にくぼんでくびれができ、その部分がちぎれて小胞(小さな袋)となることで、栄養やシグナル分子、受容体などを細胞内へ運び込む。
掲載誌:The Journal of Physical Chemistry Letters
論文タイトル:"Membrane Constriction by Dynamin through GTP-Driven Conformational Changes from Coarse-Grained Molecular Dynamics Simulations"(「粗視化分子動力学シミュレーションによるGTP駆動構造変化を介したダイナミンによる膜狭窄」)
著者:Md. Iqbal Mahmood, Shintaroh Kubo, Hiroshi Noguchi, and Kei-ichi Okazaki
掲載日:2025年11月20日(オンライン公開)
DOI:10.1021/acs.jpclett.5c02867
自然科学研究機構 分子科学研究所
星薬科大学 薬学部
東京大学 物性研究所
東京大学 医学系研究科
本研究は、JSPS科研費 基盤研究(B) (JP22H02595, JP23K23858)、学術変革領域研究(A) (JP25H02299)、若手研究 (JP22K15070)、基盤研究(C) (JP24K06973)の助成を受けたものです。
岡崎圭一(おかざきけいいち)
分子科学研究所/総合研究大学院大学 准教授
TEL:0564-55-7468
E-mail:keokazaki_at_ims.ac.jp(_at_は@に変換してください。)
自然科学研究機構 分子科学研究所 研究力強化戦略室 広報担当
TEL:0564-55-7209 FAX:0564-55-7340
E-mail:press_at_ims.ac.jp(_at_は@に変換してください。)
総合研究大学院大学 総合企画課 広報社会連携係
TEL:046-858-1629
E-mail:kouhou1_at_ml.soken.ac.jp(_at_は@に変換してください。)