サイト内検索
分子研について
研究情報
共同利用案内
- 共同研究・施設利用案内
- 申請概要
- 共同研究受入研究室・利用装置一覧
- WEB申請
大学院
- 大学院教育
- 大学院案内
- 受験生向け情報
- 他大学の学生の受け入れ
- 在校生向け情報
研究・研究者
研究グループ詳細
グループリーダー

生体分子機械の作動原理、設計原理の徹底的理解
生体分子機械、生体分子モーター、1分子計測、分子機械設計、生体制御
生命活動は進化の過程で創られた分子機械が支えています1)。タンパク質でできた生体分子機械は、2016年ノーベル化学賞で話題となった人工分子機械よりも遥かに優れた機能を発揮しますが、人工分子機械のように人間が自在に設計することはまだできていません。私たちは、個々の生体分子機械の動きや形を観る、天然にない生体分子機械を創る方法を開発する、といったアプローチで、その作動原理と設計原理を明らかにします。
1.生体分子機械に学ぶ:私たちは生体分子機械の作動原理を解明します。生体分子機械の代表例は、入力エネルギーを一方向性の運動に変換する分子モーターです。私たちはリニア分子モーター2-8)や回転分子モーター9-11)を研究しています。例えば、バイオ燃料の原料となる結晶性多糖を分解するキチナーゼ3-5)、V-ATPase9-12)は一方向に運動するリニア分子モーターです。駆動力はATPではなくレールである多糖の分解のエネルギーで、ミオシン、キネシン等の従来のリニア分子モーターとは作動原理が全く異なります。また回転分子モーターV-ATPaseは9-12)、力学的回転を介してATPの化学エネルギーとイオンの電気化学ポテンシャルを相互変換することができます。これらは人工分子機械には達成できていない高度な機能です。
2.生体分子機械を創る:私たちは天然に存在しない新しい生体分子機械を創ることにチャレンジしています13),14)。生体分子機械には基本構造がよく似たものが存在します。AAA+ファミリーはその代表例です10)。網羅的変異体作製とロボットによる自動化13)、異種分子、人工分子とのハイブリッド化14)、計算科学による合理設計を駆使し、V-ATPase、キネシンなどを積極的に改造して多彩な機能を発揮する設計原理を理解します。
3.生体分子機械の機能を調べる、形を調べる:私たちは1分子計測法を生体分子機械の機能解析に駆使します15-17)。プラズモニックナノプローブを用いた高速・高位置決定精度1分子計測の開発を行っています。また、共同研究で、生体分子機械の形を調べる構造解析も行っています。
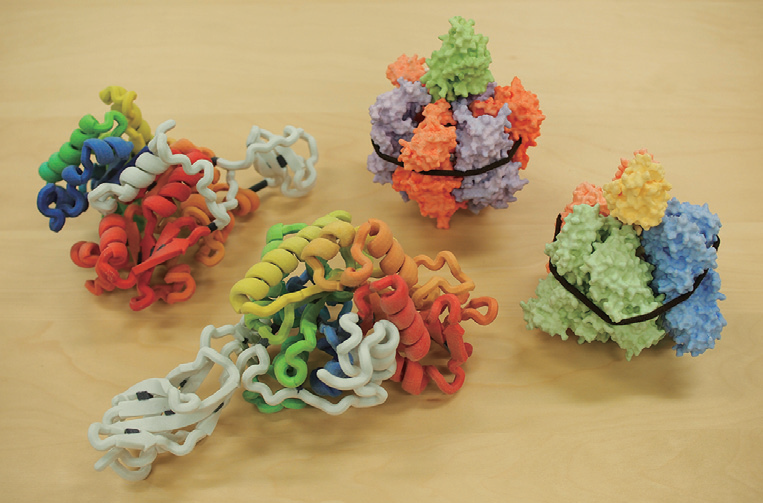
Protein molecular machines