サイト内検索
分子研について
研究情報
共同利用案内
- 共同研究・施設利用案内
- 申請概要
- 共同研究受入研究室・利用装置一覧
- WEB申請
大学院
- 大学院教育
- 大学院案内
- 受験生向け情報
- 他大学の学生の受け入れ
- 在校生向け情報
研究・研究者
研究グループ詳細
グループリーダー

固体核磁気共鳴法による生体分子・分子材料の解析
固体NMR、膜タンパク質、脂質、測定法開発、ハードウエア開発
核磁気共鳴法(NMR)は原子核の持つ磁気モーメントが磁場中で小さい磁石として振舞う性質を利用して、測定対象にラジオ波領域の電磁波を照射することにより非破壊で物質内部の分子の詳細な構造や運動性に関する原子分解能での情報を得ることができます。固体NMRは物理学者によってその基礎が築かれ、物理化学者によって化学的情報を得る手段として方法論が発展してきました。固体NMRは結晶や液晶から、粉末のようなアモルファス試料や粘性の高い液状試料まで非常に多様な物質に対して適用可能であり、特に生体分子への適用が注目されています。
当研究グループでは分子に関する様々な情報を得るための新規固体NMR測定法の開発を行っています。NMRで観測する内部相互作用には、静磁場に対する分子の相対角度を変化させる空間項の変調および、特定の強度、時間間隔でのラジオ波照射により核スピン角運動量項への外部摂動を与えることが可能です。そのため、これらの外部摂動を適切に組み合わせる実験をデザインして特定の内部相互作用を選択的に消去、復活させることが可能です。それら内部相互作用の精密な観測、解析により原子間距離や角度情報等の分子の幾何情報を得ることが出来ます。さらに緩和時間やスペクトル線形解析から特定の時間領域の分子運動性を同定することが可能です。
これまで、分子の立体構造決定に有効な精密原子間距離測定法の原理的な問題の解析1)、低発熱型感度向上法2)、および角度測定法の開発3)を行いました。さらに脂質との相互作用により機能する膜タンパク質として、インフルエンザウイルスA由来の+Hチャンネル4)、膜表在性タンパク質フォスフォリパーゼC-δ1脂質結合ドメインの機能発現機構解析5)、アルツハイマー病に関与するアミロイドβの脂質膜上で形成される会合体の構造解析6)などを行ってきました。さらに絹7)などの生体高分子材料、合成高分子複合体の構造解析8)など所内外の複数の研究機関と共同研究も行っています。
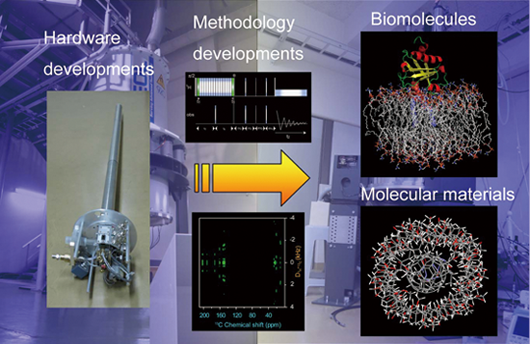
Outline of our studies.